

非小細(xì)胞靶向藥物前景如何?
2017-09-06 作者:
肺癌是我國(guó)死亡率和發(fā)病率均排名第一的惡性腫瘤疾病,根據(jù)國(guó)家癌癥中心2015年的統(tǒng)計(jì)數(shù)據(jù),我國(guó)每年新發(fā)肺癌病例約為70萬(wàn)。據(jù)商業(yè)情報(bào)供應(yīng)商 GBI Research稱,全球非小細(xì)胞肺癌治療市場(chǎng)規(guī)模將從2014年的69億美元增長(zhǎng)到 2021年的109億美元。而中國(guó)抗肺癌藥物市場(chǎng)規(guī)模早已超過(guò)200億元。
肺癌主要分為非小細(xì)胞癌和小細(xì)胞癌兩大類型,其中,非小細(xì)胞癌(NSCLC)占85%以上。隨著分子生物學(xué)的發(fā)展,多種基因突變與表達(dá)異常等分子機(jī)制被證實(shí)與NSCLC的發(fā)病、耐藥相關(guān)。目前,多種分子靶向治療藥物已投入臨床使用或正在進(jìn)行臨床試驗(yàn)。狹義上講,肺癌的靶向治療就是在細(xì)胞分子水平上,針對(duì)這些驅(qū)動(dòng)基因開發(fā)靶向藥物,定點(diǎn)抑制致癌分子,滅殺腫瘤細(xì)胞。近十年來(lái),分子靶向治療在具有驅(qū)動(dòng)基因的晚期非小細(xì)胞肺癌患者中取得顯著療效,其中,最具代表性的是針對(duì)表皮生長(zhǎng)因子受體(EGFR)和ALK基因重排的靶向治療。
本文將主要探討國(guó)內(nèi)外已上市及在研的靶向EGFR基因突變、ALK基因重排的分子靶向藥情況,歡迎指正。
一、 行業(yè)概述
1、NSCLC靶向治療靶點(diǎn)
2016年,Oncotarget雜志發(fā)表的關(guān)于1770位中國(guó)非小細(xì)胞肺癌患者大規(guī)模基因檢測(cè)結(jié)果顯示約69%的NSCLC患者攜帶驅(qū)動(dòng)基因突變。其中約58%的NSCLC患者可接受已上市藥物的靶向治療并從中獲益。
中國(guó)非小細(xì)胞肺癌靶點(diǎn)分布:
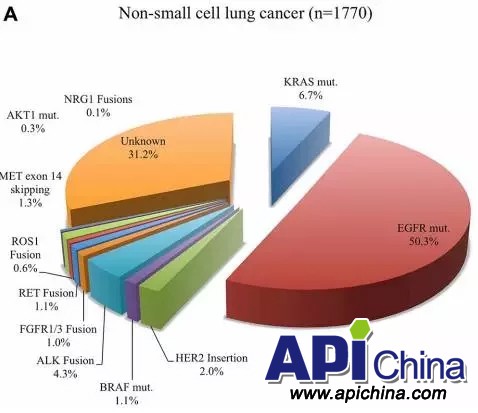
資料來(lái)源:Oncotarget.2016 Jul 5;7(27):41691-41702
肺腺癌 ( lung adenocarcinoma )是肺癌的一種,屬于非小細(xì)胞癌,占NSCLC的50%以上。下圖統(tǒng)計(jì)了肺腺癌相關(guān)的異常基因及其在肺腺癌中的發(fā)生率。目前靶向EGFR和ALK基因的分子靶向藥物可以治療約25%肺腺癌患者,仍有大量肺腺癌患者攜帶的基因突變無(wú)法通過(guò)分子靶向藥物治療,包括KRAS突變以及未知突變。
肺腺癌靶點(diǎn)分布:
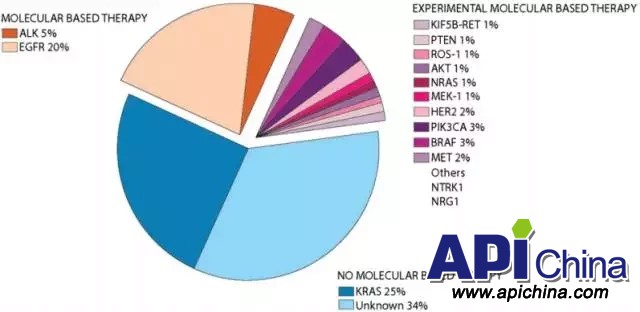
資料來(lái)源:Chest. 2014 Dec;146(6):1649-1657
2、酪氨酸激酶抑制劑靶點(diǎn)
最早被FDA批準(zhǔn)的治療肺腺癌的靶向藥物靶點(diǎn)為EGFR的酪氨酸激酶區(qū)突變者與ALK重排者。兩種藥物通常被稱為酪氨酸激酶抑制劑(以下簡(jiǎn)稱TKI)。其靶點(diǎn)情況具體如下:
(1) EGFR突變
EGFR 突變是 NSCLC 最常見(jiàn)的驅(qū)動(dòng)基因,大約20%的肺腺癌患者發(fā)生EGFR突變,約10%的高加索NSCLC患者和30-40%的東亞NSCLC患者存在EGFR突變,EGFR突變?cè)诓晃鼰煼蜗侔┗颊咧邪l(fā)生率較高。多數(shù)突變發(fā)生在EGFR激酶區(qū)的18-21號(hào)外顯子(表1)。
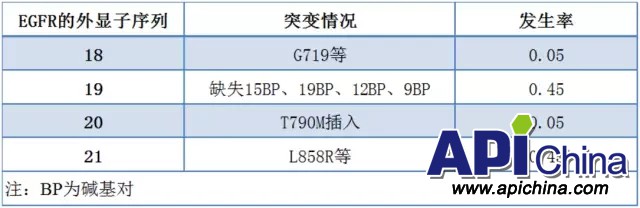
表1 EGFR的主要突變情況
最常見(jiàn)的兩種EGFR突變?yōu)?9號(hào)外顯子缺失(編碼E746-A750的15個(gè)堿基對(duì)缺失)和21號(hào)外顯子的突變L858R,在TKI敏感的腺癌中,占約90%。其它對(duì)TKI敏感的突變有21號(hào)外顯子L816Q,18號(hào)外顯子G719X。20號(hào)外顯子T790M突變與TKI原發(fā)、繼發(fā)耐藥有關(guān),此外,TKI原發(fā)耐藥與KRAS突變和ALK基因重排相關(guān),繼發(fā)耐藥與組織學(xué)轉(zhuǎn)化(NSCLC轉(zhuǎn)化為SCLC、EMT)有關(guān)。另一個(gè)耐藥機(jī)制是MET擴(kuò)增,通過(guò)ERBB3信號(hào)導(dǎo)致了PIK3CA/AKT 通路激活,出現(xiàn)在大約1%-2%的肺腺癌患者中,為5% -20%的TKI耐藥負(fù)責(zé)。腫瘤中的其它基因相互作用,比如EGFR信號(hào)通路的下游基因的突變,HER2擴(kuò)增,也導(dǎo)致TKI耐藥。
(2) ALK重排
EML4-ALK融合基因發(fā)生于接近5%的肺腺癌患者中,導(dǎo)致被EML4編碼的蛋白的N端和被ALK編碼的受體酪氨酸激酶的跨膜信號(hào)部分融合。ALK的激活導(dǎo)致細(xì)胞增殖、存活、遷移和細(xì)胞骨架重組的改變。EML4-ALK融合的患者有一些特殊的臨床和病理特點(diǎn),比如年齡較年輕,從不吸煙,進(jìn)展期,低分化,固體和篩型組織,帶有粘液和印戒細(xì)胞樣特點(diǎn)等。
3、其他潛在的靶點(diǎn)
(1) ROS1融合突變
在約 1%~2% 的 NSCLC 中可檢測(cè)到 ROS1 重排,導(dǎo)致了通路的連續(xù)激活。ROS1 是胰島素受體家族的一種受體酪氨酸激酶。重排通常表現(xiàn)為CD74和SLC 34A2 ,這個(gè)重排在腺癌中的發(fā)生率為1%,克唑替尼被認(rèn)為在攜帶ROS-1融合基因的腫瘤中具有活性。ALK和ROS1的激酶活性區(qū)域有70%的相似性,因此ALK的抑制劑很多是可以用于ROS1的治療的。
(2) KRAS突變
KRAS 突變存在于15%~20%的NSCLC,存在于大約25%的肺腺癌中。KRAS 是RAS GTP酶家族的成員之一,可以通過(guò)Ras/Raf信號(hào)通路促進(jìn)細(xì)胞的生長(zhǎng)分化。該突變與吸煙史有明顯的相關(guān)性。突變的KRAS與GTP的高親和性限制了直接抑制KRAS的藥物的研發(fā)和應(yīng)用,暫時(shí)沒(méi)有特異性的治療藥物。
(3) PIK3CA/AKT/mTOR通路突變
該通路突變包括PIK3CA、AKT、PTEN突變,這些突變出現(xiàn)在腺癌和鱗癌中,PIK3CA突變是致癌的,在這個(gè)群組中最常見(jiàn),并可與腺癌的其它突變共存。PIK3CA/AKT/mTOR通路突變?cè)黾恿薽TOR抑制劑依維莫司的敏感性。然而,早期臨床試驗(yàn)顯示靶向這個(gè)通路的藥物僅有部分反應(yīng)。
(4) BRAF突變
BRAF屬于MAPK 信號(hào)通路的絲氨酸蘇氨酸蛋白激酶家族,約1%~3%的 NSCLC存在BRAF突變。在肺癌中,研究者檢測(cè)到了BRAF 的多種突變位點(diǎn),如 V600E(50%)、G469A(40%)、D594G(11%)。
(5) HER2突變
約 2%~4% 的NSCLC患者存在HER2突變,多數(shù)患者具有不吸煙腺癌的臨床特征,最常見(jiàn)的突變類型是發(fā)生于20外顯子的插入突變A775_G776ins YVMA,而在EGFR/KRAS/ALK均陰性的NSCLC穿刺標(biāo)本中,HER2突變的發(fā)生率為6%。
(6) NTRK1和NRG1重排
近來(lái),兩個(gè)新的改變被發(fā)現(xiàn):NTRK1和NRG1重排。NTRK1是編碼高親和性神經(jīng)生長(zhǎng)因子(TRKA蛋白)的基因。研究發(fā)現(xiàn),NTRK1融合基因存在于3%的沒(méi)有其它突變的腺癌患者中,而NRG1重排似乎主要存在于侵襲性腺癌。兩個(gè)突變可能成為特異性的藥物靶點(diǎn)。
在所有NSCLC分子靶向治療靶點(diǎn)中,EGFR和ALK變異仍然是主要的兩個(gè)類型,本文主要針對(duì)EGFR-TKIs和ALK-TKIs進(jìn)行詳細(xì)分析。
二、EGFR-TKIs藥物
EGFR是HER/ErbB家族重要成員,它廣泛分布于人體各類組織的細(xì)胞膜上,其結(jié)構(gòu)分為胞外區(qū)、跨膜區(qū)及胞內(nèi)區(qū)。
EGFR受體家族激活機(jī)制:
資料來(lái)源:The Oncologist August 15, 2002 vol. 7
當(dāng)EGFR受體受到相應(yīng)配體的作用后,可誘導(dǎo)受體形成同型或者異型二聚體,引起胞外結(jié)構(gòu)發(fā)生構(gòu)象變化,進(jìn)而激活胞內(nèi)區(qū)酪氨酸激酶,使其殘基磷酸化,進(jìn)一步激活下游信號(hào)通路,如MARK通路及PI3K通路等,最終導(dǎo)致腫瘤發(fā)生一系列生物學(xué)行為,如腫瘤的發(fā)生發(fā)展、增殖、侵襲及轉(zhuǎn)移等。
EGFR酪氨酸激酶抑制劑(tyrosine-kinase-inhibitor,TKI)是一種小分子EGFR抑制劑,它們通過(guò)內(nèi)源性配體競(jìng)爭(zhēng)性結(jié)合EGFR,抑制酪氨酸激酶的活化,進(jìn)而阻斷EGFR信號(hào)通路,最終產(chǎn)生抑制腫瘤細(xì)胞的增殖、轉(zhuǎn)移并促進(jìn)腫瘤細(xì)胞發(fā)生凋亡等一系列生物學(xué)效應(yīng)。
EGFR激酶區(qū)活化突變是EGFR-TKI的最重要的療效預(yù)測(cè)因子,EGFR突變主要發(fā)生在18~21號(hào)外顯子,其中19號(hào)外顯子的缺失突變和21號(hào)外顯子的L858R點(diǎn)突變是最常見(jiàn)的EGFR突變亞型,占所有突變類型的90%,稱為EGFR基因的敏感突變。
第一個(gè)上市的EGFR-TKI是吉非替尼。一項(xiàng)比較吉非替尼和含鉑雙藥方案在肺腺癌中療效的Ⅲ期臨床隨機(jī)對(duì)照臨床試驗(yàn)叫做IPASS研究 ,該研究開啟了EGFR-TKI的肺癌精準(zhǔn)醫(yī)學(xué)時(shí)代,堪稱肺癌靶向治療的里程碑。自那以來(lái),EGFR-TKI發(fā)展到了三代(表2)。
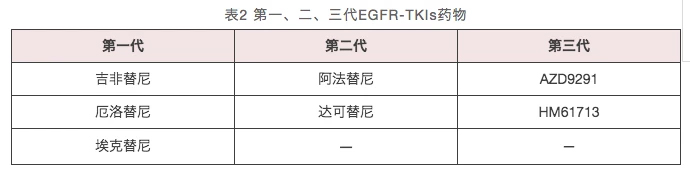
1、 第一代EGFR-TKIs
IPASS研究首次證明EGFR突變狀態(tài)是肺癌患者對(duì)吉非替尼療效的強(qiáng)預(yù)測(cè)因子,奠定了肺癌分子靶向治療的基石。
隨后,多項(xiàng)大型Ⅲ期隨機(jī)對(duì)照臨床研究如First-SIGNAL、WJT0G3405、NEJ002、OPTIMAL、ENSURE和EURTAC相繼證實(shí),存在EGFR突變的肺癌患者接受EGFR-TKIs療效顯著優(yōu)于傳統(tǒng)化療,一線治療的中位PFS可達(dá)9~13個(gè)月,客觀緩解率(objective response rate,ORR)為60%~85%,且不良反應(yīng)及生活質(zhì)量要顯著優(yōu)于化療(表3)。
因此,一代EGFR-TKI已成為伴EGFR基因敏感突變陽(yáng)性晚期非小細(xì)胞肺癌的標(biāo)準(zhǔn)一線治療。
表3 一代EGFR-TKI治療EGFR突變陽(yáng)性患者的經(jīng)典臨床研究:
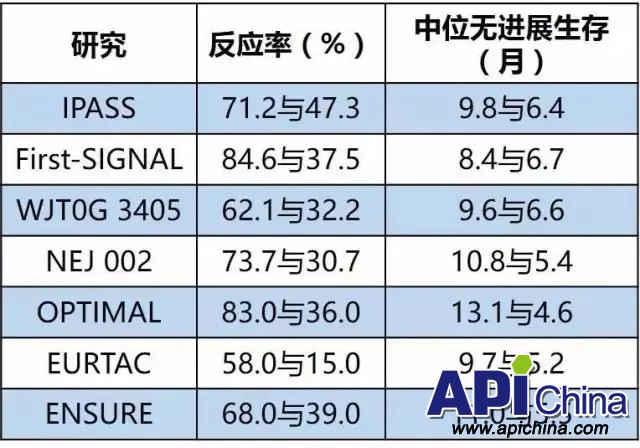
目前,國(guó)內(nèi)的一代EGFR-TKI主要包括吉非替尼、厄洛替尼以及埃克替尼。吉非替尼于2005年中國(guó)上市,隨即厄洛替尼、埃克替尼分別于2007年、2011年在中國(guó)上市。
總而言之,一代EGFR-TKI冶療初期的EGFR基因突變陽(yáng)性患者,ORR及PFS均顯著優(yōu)于標(biāo)準(zhǔn)化療。而關(guān)于一代EGFR-TKI的研究均提示,三種靶向藥物的療效相似,但吉非替尼皮疹的發(fā)生率較低。
2、第二代EGFR-TKI
阿法替尼是第二代的靶向治療藥物,是針對(duì)ErbB家族的不可逆性阻滯劑,其可以選擇且有效地阻滯ErbB家族受體(如EGFR,HER2,HER4)的信號(hào)傳導(dǎo)以及ErbB的磷酸轉(zhuǎn)移。與可逆性的EGFR酪氨酸激酶抑制劑(如吉非替尼和厄洛替尼)不同,二代EGFR-TKI能與ErbB受體網(wǎng)絡(luò)形成共價(jià)結(jié)合,不可逆的、完全中斷信號(hào)傳導(dǎo),從而帶來(lái)持續(xù)且廣譜的抗有絲分裂活性。
雖然在一代EGFR-TKI中,EGFR基因突變陽(yáng)性患者可從中獲得約10個(gè)月的中位緩解時(shí)間,但其獲得性耐藥問(wèn)題仍有待解決,其最重要的分子機(jī)制是發(fā)生在EGFR基因20號(hào)外顯子發(fā)生T790M二次突變。
而阿法替尼與ErbB家族受體不可逆結(jié)合的特性理論上會(huì)在一定程度上克服由T790M突變導(dǎo)致的獲得性耐藥。除了阿法替尼外,達(dá)克替尼(Dacomitinib)也是第二代EGFR-TKI中的另一代表性藥物。
第二代EGFR-TKI再次驗(yàn)證了EGFR-TKI相比標(biāo)準(zhǔn)化療的優(yōu)勢(shì),同時(shí)細(xì)化了EGFR基因突變不同類型間的療效差異,藥物療效似乎比一代藥物更優(yōu)。雖然在體外對(duì)突變患者有活性,但臨床未能克服突變產(chǎn)生耐藥性,毒副反應(yīng)更加令人堪憂,因此,第二代的靶向藥臨床運(yùn)用并不廣泛。
3、第三代EGFR-TKIs
盡管一代、二代分子靶向藥物都獲得顯著延長(zhǎng)的中位緩解時(shí)間,但絕大部分患者最終會(huì)產(chǎn)生耐藥,其中出現(xiàn)T790M二次突變占了所有耐藥機(jī)制的50%~60%。
第三代EGFR-TKI是一種高度選擇性、有效對(duì)抗EGFR-TKI獲得性T790M耐藥的新一代靶向治療藥物, AZD9291(Osimertinib)、HM6171(Olmutinib)等三代靶向藥物橫空出世,為克服TKI獲得性耐藥開啟了全新的篇章。目前,除已經(jīng)上市的兩款三代EGFR-TKI藥物外,國(guó)內(nèi)外有大量三代藥正處于開發(fā)之中。
(1) 國(guó)外情況
AZD9291于2015年11月中旬獲美國(guó)FDA的加速批準(zhǔn)用于T790M突變陽(yáng)性轉(zhuǎn)移性NSCLC的治療,隨后歐盟也加速批準(zhǔn)了此項(xiàng)適應(yīng)證,這些進(jìn)展主要是基于2個(gè)Ⅱ期研究(AURA拓展研究及AURA2研究)以及AURAⅠ期拓展研究的積極數(shù)據(jù)。同樣,AZD9291—線治療EGFR突變陽(yáng)性NSCLC顯示出令人鼓舞的臨床活性和良好的安全性。從目前的臨床研究數(shù)據(jù)看來(lái),三代靶向藥物對(duì)一代TKI進(jìn)展且伴T790M突變陽(yáng)性患者的療效顯著,其中AZD9291是目前唯一獲FDA批準(zhǔn)上市的三代藥物(表4)。
國(guó)外第三代EGFR抑制劑研發(fā)情況:
藥品名稱:Osimertinib (奧希替尼,AZD9291)
公司:阿斯利康
簡(jiǎn)介:口服突變選擇性不可逆EGFR抑制劑,對(duì)EGFR-TKI敏感型及T790耐藥突變有效,獲批治療EGFR T790突變陽(yáng)性非小細(xì)胞肺癌。
階段:2015年11月和2016年2月分別獲得FDA和EMA上市批準(zhǔn)。2016年3月日本批準(zhǔn),2017年獲CFDA批準(zhǔn)。
代表試驗(yàn):AURA系列試驗(yàn)
實(shí)驗(yàn)數(shù)據(jù):
有效性:AURA3 III期研究數(shù)據(jù)顯示,Tagrisso (osimertinib,AZD9291)作為二線療法相比含鉑類藥物的二聯(lián)標(biāo)準(zhǔn)化療可使無(wú)進(jìn)展生存期顯著延長(zhǎng)5.7個(gè)月(10.1 vs 4.4個(gè)月)。AURA3研究中,基線時(shí)有34%的患者發(fā)生中樞神經(jīng)系統(tǒng)轉(zhuǎn)移。對(duì)于這部分患者,Tagrisso治療組的PFS相比含鉑類藥物的二聯(lián)標(biāo)準(zhǔn)化療也有顯著改善(8.5 vs 4.2個(gè)月)。
安全性:AURA3研究結(jié)果與之前的研究數(shù)據(jù)一致。Tagrisso 治療組3級(jí)以上的藥物治療相關(guān)不良事件發(fā)生率為6%(n=16),鉑類藥物化療組為34%(n=46)。Tagrisso組其他常見(jiàn)藥物相關(guān)不良反應(yīng)包括腹瀉(29%),皮疹(28%);化療組其他常見(jiàn)不良反應(yīng)包括惡心(47%)和食欲不振(32%)。
藥品名稱:Olmutinib (奧莫替尼)
公司:韓美、BI、再鼎醫(yī)藥
簡(jiǎn)介:
Olmutinib于2016年5月獲韓國(guó)MFDS批準(zhǔn)上市,最初由韓美制藥研發(fā),2015年7月授權(quán)給勃林格殷格翰除韓國(guó)、中國(guó)和香港以外地區(qū)的全球研發(fā)和商業(yè)化權(quán)利,2015年11月再鼎醫(yī)藥獲得中國(guó)地區(qū)(包括香港和澳門)的研發(fā)、生產(chǎn)及商業(yè)化權(quán)利。奧莫替尼用于治療晚期或轉(zhuǎn)移性T790M突變陽(yáng)性非小細(xì)胞肺癌。
階段:在韓國(guó)上市、再鼎2016年5月提交CFDA臨床申請(qǐng),BI已經(jīng)放棄研發(fā)。
代表試驗(yàn):HM-EMSI-101試驗(yàn)
實(shí)驗(yàn)數(shù)據(jù):
有效性:I/II期試驗(yàn)中,ORR達(dá)62%,疾病控制率為91%。
不良反應(yīng):10%以上患者出現(xiàn)的藥物相關(guān)不良反應(yīng)包括脫皮、惡心、腹瀉、皮疹、納差、瘙癢、頭痛等;多數(shù)不良反應(yīng)為1/2度,容易控制或停藥后緩解。2016年10月韓國(guó)2名患者死亡。
藥品名稱:Rociletinib Hydrobromide
公司:Celgene,Clovis
簡(jiǎn)介:
是由Avila公司原研的小分子化合物,其中Avila于2011年被新基收購(gòu)。該藥由新基和Clovis共同開發(fā)。口服靶向結(jié)合于敏感型EGFR基因突變以及T790M突變
階段:
2015年7月FDA否決上市申請(qǐng)。Clovis撤回歐盟上市申請(qǐng)。
2016Q1放棄研發(fā)。
代表試驗(yàn):TIGER系列試驗(yàn)
實(shí)驗(yàn)數(shù)據(jù):
有效性:ORR為30%,低于開始公布的60%。劑量從500毫克提高到625毫克缺乏PK研究支持。
不良反應(yīng):惡心(34%),腹瀉(23%)、糖耐量異常/高血糖癥(52%),嘔吐(17%),肌肉酸痛(11%),QTc間期延長(zhǎng)(15%)。
藥品名稱:Nazartinib EGF816
公司:諾華
簡(jiǎn)介:
Nazartinib是諾華公司研發(fā)的第三代小分子口服EGFR不可逆抑制劑,目前處于2期臨床試驗(yàn)中。類似于AZD9291,Nazartinib也是氨基嘧啶結(jié)構(gòu),共價(jià)結(jié)合于EGFR催化域ATP結(jié)合位點(diǎn)邊緣的C797,對(duì)T790M突變有很強(qiáng)抑制活性。
階段:臨床II期
代表試驗(yàn):NCT02108964
實(shí)驗(yàn)數(shù)據(jù):
有效性:臨床I期中,入組了132名T790M陽(yáng)性NSCLC患者(排除有進(jìn)展的腦轉(zhuǎn)移),ORR44%,疾病控制率91%,中位PFS9.2月。
不良反應(yīng):腹瀉(40%)、皮疹(39%)、皮膚瘙癢(32%)、皮膚干燥(23%)、口腔炎(23%)、疲勞(21%);估計(jì)最大耐受劑量小于225mg每天。
藥品名稱:Naquotinib(ASP8273)
簡(jiǎn)介:
Naquotinib是安斯泰來(lái)原研的治療EGFR突變的非小細(xì)胞肺癌的藥物。在日本開展的幾起臨床試驗(yàn)結(jié)果顯示,Naquotinib能有效控制腫瘤縮小,且副作用較小
階段:臨床III期終止
代表試驗(yàn):SOLAR試驗(yàn)
實(shí)驗(yàn)數(shù)據(jù):
有效性:I期中,所有劑量ORR46.9%,中位PFS9.7月。安全性:副作用比AZD9291低。
2017年5月,Astellas 宣布終止公司 EGFR T790M 抑制劑 ASP8273 的 III 期 SOLAR 試驗(yàn),試驗(yàn)將停止入組新患者。
從國(guó)外大型藥企研發(fā)進(jìn)度來(lái)看,其他的三代藥物如CO-1686、BI1482694、EGF816、ASP8273等產(chǎn)品中,CO-1686(Rociletinib)于2015年7月被FDA否決上市申請(qǐng)。Clovis后來(lái)撤回歐盟上市申請(qǐng),于2016年一季度放棄研發(fā);諾華公司的EGF816目前正處于II期臨床研究中;Olmutinib(HM61713/BI1482694)于2016年5月獲韓國(guó)MFDS批準(zhǔn)上市,最初由韓美制藥研發(fā),2015年7月授權(quán)給勃林格殷格翰除韓國(guó)、中國(guó)和香港以外地區(qū)的全球研發(fā)和商業(yè)化權(quán)利,2015年11月再鼎醫(yī)藥獲得中國(guó)地區(qū)(包括香港和澳門)的研發(fā)、生產(chǎn)及商業(yè)化權(quán)利。但該藥在2016年10月導(dǎo)致韓國(guó)2名患者死亡。Naquotinib(ASP8273)是安斯泰來(lái)原研的治療EGFR突變的非小細(xì)胞肺癌的藥物。在日本開展的幾起臨床試驗(yàn)結(jié)果顯示,Naquotinib能有效控制腫瘤縮小,且副作用較小,但目前臨床III期試驗(yàn)已經(jīng)終止。
(2) 國(guó)內(nèi)情況
國(guó)內(nèi)市場(chǎng)來(lái)看,阿斯利康公司于2017年3月24日宣布,CFDA已正式批準(zhǔn)第三代肺癌靶向藥物泰瑞沙(甲磺酸奧希替尼片, AZD9291)用于既往經(jīng)表皮生長(zhǎng)因子受體(EGFR)酪氨酸激酶抑制劑(TKI)治療時(shí)或治療后出現(xiàn)的疾病進(jìn)展,并且經(jīng)檢測(cè)確認(rèn)存在EGFR T790M突變陽(yáng)性的局部晚期或轉(zhuǎn)移性非小細(xì)胞性肺癌(NSCLC)成人患者的治療。
國(guó)內(nèi)正在研發(fā)三代藥物的企業(yè)及產(chǎn)品(表5)包括,艾森生物的艾維替尼目前處于臨床II/III期試驗(yàn)階段;貝達(dá)藥業(yè)的BPI-7711和BPI-15086處于臨床I期研究階段;上海艾力斯處于臨床I期研究階段;江蘇豪森的HS-10296處于國(guó)際多中心臨床I/II期階段,并獲批CFDA臨床批件。GMA204為第三代酪氨酸激酶抑制劑,分子量小,可以透過(guò)血腦屏障(BBB),在動(dòng)物腦內(nèi)藥物分布比例高于EGFR的其他TKIs,對(duì)擴(kuò)增的原發(fā)性腫瘤腦轉(zhuǎn)移患者,療效可能會(huì)優(yōu)于現(xiàn)有已上市的酪氨酸酶抑制劑(TKIs)。GMA204由鴻運(yùn)華寧和蘇州韜略聯(lián)合申報(bào),在2016年12月批準(zhǔn)臨床。揚(yáng)子江海雁藥業(yè)的YZJ-0318目前處于臨床1期,華東醫(yī)藥的邁華替尼也處于臨床I期。總體來(lái)看,在當(dāng)前AZD9291已經(jīng)中國(guó)獲批上市的情況下,國(guó)內(nèi)企業(yè)只有臨床效果優(yōu)于AZD9291或者能夠穿過(guò)血腦屏障的藥物才具備較大的投資價(jià)值。
國(guó)內(nèi)三代EGFR抑制劑研發(fā)情況
藥品名稱:艾維替尼AC0010
公司:艾森生物
簡(jiǎn)介:
口服突變選擇性不可逆EGFR抑制劑,對(duì)EGFR-TKI敏感型及T790M耐藥突變有效。
階段:臨床II/III期
代表試驗(yàn):AC0010人體試驗(yàn)
實(shí)驗(yàn)數(shù)據(jù):
有效性:初步結(jié)果,總體ORR為38.2%,T790M陽(yáng)性的病人有效劑量范圍內(nèi)ORR62%。
不良反應(yīng):腹瀉(44%)、皮疹(20%)、瘙癢(16%)、腹瀉和皮疹的頻率增加呈劑量依賴性
藥品名稱:
Alflutinib Mesylate AST2818
公司:上海艾力斯
簡(jiǎn)介:
甲磺酸艾氟替尼是一種潛在治療晚期非小細(xì)胞肺癌(NSCLC)的第三代針對(duì)EGFR T790M突變的抑制劑。
階段:臨床I期
代表試驗(yàn):臨床前試驗(yàn)
實(shí)驗(yàn)數(shù)據(jù):
對(duì)T790M耐藥腫瘤展現(xiàn)良好的抑制腫瘤活性;該藥在動(dòng)物體內(nèi)分布廣泛,并可以通過(guò)血腦屏障。該藥在臨床前研究未發(fā)現(xiàn)心臟毒性,眼毒性和高血糖等不良反應(yīng),已展現(xiàn)良好的安全性。
藥品名稱:
BPI-7711/ BPI-15086
公司:貝達(dá)藥業(yè)
簡(jiǎn)介:
一種潛在的治療T790M突變的非小細(xì)胞肺癌(NSCLC)的第三代表皮生長(zhǎng)因子受體(EGFR)抑制劑。
階段:臨床I期
實(shí)驗(yàn)數(shù)據(jù):無(wú)。
藥品名稱:
HS-10296
公司:江蘇豪森
簡(jiǎn)介:
HS-10296是豪森最新研發(fā)的治療肺癌的第三代分子靶向藥物,針對(duì)EGFR-T790M突變這個(gè)靶點(diǎn)。針對(duì)這個(gè)藥物的治療優(yōu)勢(shì)和良好的開發(fā)前景,豪森藥業(yè)制定了國(guó)內(nèi)國(guó)外同時(shí)申報(bào)的開發(fā)策略。目前已經(jīng)在美國(guó)、臺(tái)灣、韓國(guó)三個(gè)國(guó)家和地區(qū)的開展國(guó)際多中心臨床研究。
階段:
國(guó)際多中心臨床1/2期,CFDA獲批臨床。
代表試驗(yàn):臨床前試驗(yàn)
實(shí)驗(yàn)數(shù)據(jù):
據(jù)了解其在體內(nèi)的活性是同類藥品的2倍。由于它有獨(dú)特的分子結(jié)構(gòu)和獨(dú)特的代謝途徑,可以很好地規(guī)避嚴(yán)重皮疹和胃腸道毒性等不良反應(yīng),能解決現(xiàn)有藥物的技術(shù)難題。
藥品名稱:
GMA204
公司:鴻運(yùn)華寧&韜略生物
簡(jiǎn)介:
GMA204屬于擁有自主知識(shí)產(chǎn)權(quán)的1.1類新藥,其作為新一代的酪氨酸激酶抑制劑,分子量小,可以透過(guò)血腦屏障(BBB)。
階段:臨床I期
代表試驗(yàn):臨床前試驗(yàn)
實(shí)驗(yàn)數(shù)據(jù):
在動(dòng)物腦內(nèi)藥物分布比例高于EGFR的其他TKIs,對(duì)擴(kuò)增的原發(fā)性腫瘤腦轉(zhuǎn)移患者療效可能優(yōu)于已上市的TKIs。同時(shí),其對(duì)EGFR的抑制作用比可逆性抑制劑更強(qiáng),可作用于多種HER通道的受體,能同時(shí)抑制野生型的EGFR受體以及新突變EGFR受體(T790M變異),臨床應(yīng)用于EGFR突變的NSCLC,可針對(duì)化療無(wú)效或者第一代EGFR抑制劑產(chǎn)生耐藥性和產(chǎn)生新的T790M變異的晚期患者。
藥品名稱:
YZJ-0318
公司:揚(yáng)子江海雁藥業(yè)
簡(jiǎn)介:
獨(dú)立開發(fā)的第三代表皮生長(zhǎng)因子受體(EGFR)抑制劑,它可用于治療在第一代EGFR抑制劑吉非替尼或厄洛替尼治療后出現(xiàn)T790M耐藥突變的非小細(xì)胞肺癌病人。
階段:獲批臨床
代表試驗(yàn):臨床前試驗(yàn)
實(shí)驗(yàn)數(shù)據(jù):
該候選藥物能夠選擇性的抑制T790M耐藥突變,在含有T790M突變的H1975肺癌移植瘤模型以及病人來(lái)源的含有T790M、L858R雙突變的肺癌移植瘤模型中,均能夠有效抑制腫瘤生長(zhǎng),同時(shí),它對(duì)野生型EGFR作用很弱,在EGFR野生型的A431移植瘤模型中并不抑制腫瘤生長(zhǎng),提示YZJ-0318可能在臨床上具有較小的皮疹、腹瀉及間質(zhì)肺炎的副作用。
藥品名稱:
邁華替尼
公司:華東醫(yī)藥
簡(jiǎn)介:
華東醫(yī)藥是國(guó)內(nèi)第2家申報(bào)T790M突變藥物的企業(yè)。邁華替尼片的臨床申請(qǐng)2014年3月25獲CDE受理,比艾維替尼晚了近半年時(shí)間,但是2014年10月即獲批臨床,只比艾維替尼晚了1個(gè)月。
階段:臨床I期
實(shí)驗(yàn)數(shù)據(jù):無(wú)。
臨床上針對(duì)EGFR基因敏感突變患者,應(yīng)首選EGFR-TKI冶療。目前,臨床上的一代TKI療效相當(dāng),以阿法替尼為代表的二代TKI對(duì)于突變陽(yáng)性患者也顯示出了很好的療效,但是副作用較大。
第三代TKI克服了T790M獲得性耐藥,療效卓越、安全性好,成為T790M陽(yáng)性患者的首選治療,但最佳的使用時(shí)機(jī)、次序以及新的耐藥問(wèn)題如C797S突變,仍需進(jìn)一步探索,三代TKI是否能夠取代前兩代TKI成為一線治療的探索也讓我們拭目以待。
4、 EGFR-TKIs治療NSCLC腦膜轉(zhuǎn)移
非小細(xì)胞肺癌(non-small cell lung cancer, NSCLC)患者發(fā)生腦膜轉(zhuǎn)移后,如不進(jìn)行治療,患者的生存時(shí)間僅為4~6周。盡管鞘內(nèi)注射化療藥物在晚期NSCLC腦膜轉(zhuǎn)移患者中顯示出一定的療效,但NSCLC腦膜轉(zhuǎn)移患者的生存時(shí)間仍僅為12~14周。
肺腺癌是NSCLC腦膜轉(zhuǎn)移患者主要的病理類型,約占84%~97%。其中43%~70.5%的NSCLC腦膜轉(zhuǎn)移患者檢測(cè)到EGFR敏感突變。有研究表明,經(jīng)選擇的EGFR敏感突變NSCLC患者應(yīng)用EGFR酪氨酸激酶抑制劑(TKIs)治療腦膜轉(zhuǎn)移有效,并可延長(zhǎng)患者的生存時(shí)間。其原因主要是由于EGFR-TKIs是小分子的靶向治療藥物,能透過(guò)血腦屏障。此外,EGFR-TKIs藥物不良反應(yīng)小,即使患者的美國(guó)東部腫瘤協(xié)作組評(píng)分差也可接受治療。但仍需要進(jìn)一步的臨床試驗(yàn)來(lái)驗(yàn)證EGFR-TKIs治療NSCLC腦膜轉(zhuǎn)移患者的療效。隨著EGFR-TKIs的廣泛應(yīng)用,EGFR敏感突變患者的生存時(shí)間明顯延長(zhǎng),但部分腦膜轉(zhuǎn)移出現(xiàn)在EGFR-TKIs治療之后,此類患者對(duì)于EGFR-TKIs的治療效果欠佳,其治療成為臨床工作的難點(diǎn)。
三、 ALK-TKIs藥物
1、 ALK靶點(diǎn)情況
間變性淋巴瘤激酶(ALK)基因融合突變是非小細(xì)胞肺癌(NSCLC)常見(jiàn)的一種驅(qū)動(dòng)基因,突變的形式有過(guò)量表達(dá)、形成融合基因,發(fā)生點(diǎn)突變等。ALK基因最初是1994 年在非霍奇金淋巴瘤中發(fā)現(xiàn)的,是由于染色體異位導(dǎo)致ALK 與核仁磷酸蛋白(NPM)融合所致。2007 年,Soda 等對(duì)非小細(xì)胞肺癌進(jìn)行研究時(shí)發(fā)現(xiàn)了相同的ALK 基因,但此時(shí)卻是因?yàn)槿旧w2p內(nèi)小的倒位導(dǎo)致ALK和棘皮動(dòng)物微管相關(guān)蛋白樣蛋白4(EML4)融合。EML4基因可在多個(gè)位點(diǎn)發(fā)生斷裂,與位于ALK第20外顯子的胞內(nèi)催化域相連,形成EML4-ALK融合基因。EML4斷裂位點(diǎn)不同可以與ALK形成至少10種以上的EML4-ALK融合基因變體(Variant),變體1和變體3最常見(jiàn),其他的融合伴侶基因還有KIF5B、TFG和KLC1等,目前發(fā)現(xiàn)有27種融合形式。EML4-ALK 融合型癌基因存在于高達(dá)3-5% 的NSCLC,可促進(jìn)惡性生長(zhǎng)及增殖。
非小細(xì)胞肺癌中ALK的重排形式:
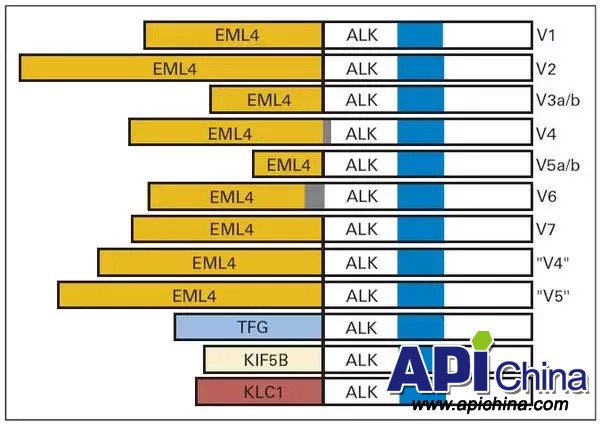
肺癌患者的福音:非小細(xì)胞靶向藥物前景如何?
中國(guó)非小細(xì)胞肺腺癌中ALK融合突變陽(yáng)性的比例為4.3%,ALK陽(yáng)性的非小細(xì)胞肺癌被認(rèn)為是是一種獨(dú)立的分子亞型,與其他驅(qū)動(dòng)基因互相排斥,相對(duì)應(yīng)的靶向藥物與EGFR分子亞型完全不同。肺鱗癌患者ALK融合基因突變概率很低,有報(bào)道說(shuō)1400個(gè)肺鱗癌患者里ALK融合基因的發(fā)生率為1.3%。相比 EGFR 來(lái)說(shuō),ALK 重排更可能見(jiàn)于特殊人群:吸煙少或不吸煙的年輕腺癌患者、組織學(xué)上多為印戒細(xì)胞者。女性具有ALK 重排的腫瘤,自然不會(huì)有EGFR 或KRAS 突變,且意味著是一種「癌基因依賴性」表型,即單一基因產(chǎn)物可導(dǎo)致惡性改變。
雖然目前有第一、第二代靶向藥物,但是ALK陽(yáng)性患者經(jīng)過(guò)開始階段的治療敏感期后不可避免地出現(xiàn)獲得性耐藥。耐藥機(jī)制包括ALK擴(kuò)增,EGFR/HER2、HER2和HER3的上調(diào),Ckit擴(kuò)增,包括L1196M在內(nèi)(如同EGFR中的T790M)的多種ALK 突變。因此,研制克服第一代、第二代ALK抑制劑弱點(diǎn),開發(fā)出療效好、副作用小的第三代ALK抑制劑治療該類癌癥具有潛在的市場(chǎng)價(jià)值。
2、現(xiàn)有藥物
治療ALK陽(yáng)性非小細(xì)胞肺癌的創(chuàng)新藥是生物制藥公司研究的熱點(diǎn)。第一代靶向藥物是克唑替尼2011年,輝瑞研制的克唑替尼上市,2016年實(shí)現(xiàn)銷售額達(dá)到1.45億美元,預(yù)計(jì)2018年將達(dá)到8.3億美元。克唑替尼耐藥后可以使用第二代ALK抑制劑,主要有色瑞替尼(LDK378)、艾樂(lè)替尼(CH5424802)、Brigatinib(AP26113)和X-396。其中,諾華研制的色瑞替尼于2014年4月29日獲FDA加速批準(zhǔn)上市,2016 年其實(shí)現(xiàn)了9100 萬(wàn)美元的銷售額。分析師預(yù)測(cè)這款藥物的年銷售峰值最終會(huì)達(dá)到大約3億美元。羅氏和中外制藥兩家公司開發(fā)的艾樂(lè)替尼Alectinib,2014年在日本上市,2015年美國(guó)上市,2015年度的銷售額為7130萬(wàn)美元。Ariad 的Brigatinib (AP26113) 一種新型的ALK和EGFR雙重抑制劑,可強(qiáng)效抑制ALK的L1196M突變和EGFR的T790M突變。Brigatinib 已于2017年4月28日獲得FDA批準(zhǔn)上市,已被證實(shí)是目前第二代ALK抑制劑中最好的產(chǎn)品。
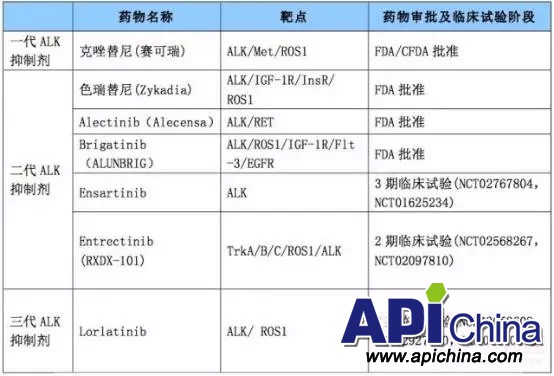
表6 第一、二、三代ALK-TKIs藥物
(1) 藥物詳細(xì)介紹
克唑替尼分別于 2011 年、2013 年通過(guò) FDA 和 CFDA 批準(zhǔn),用于 ALK 基因融合陽(yáng)性晚期 NSCLC 患者的治療。PROFILE1014 研究共納入 343 例 ALK 陽(yáng)性的 NSCLC 患者,其中分別接受克唑替尼治療和一線化療(順鉑 / 卡鉑聯(lián)合培美曲塞)。相比于一線化療組,克唑替尼組同樣顯示了較長(zhǎng)的無(wú)進(jìn)展生存期 PFS(10.9 個(gè)月對(duì)比 7.0 個(gè)月)和較高的藥物緩解率(RR)(74% 對(duì)比 45%)。
色瑞替尼于 2014 年被 FDA 批準(zhǔn),用于既往接受克唑替尼后病情進(jìn)展或?qū)诉蛱婺岵荒褪艿?ALK 陽(yáng)性晚期 NSCLC 患者的治療。2017 年 5 月底,F(xiàn)DA 批準(zhǔn)色瑞替尼用于 ALK 陽(yáng)性的晚期 NSCLC 患者的一線治療。FDA 的快速審批是基于 Ⅲ 期 ASCEND-4 臨床研究的結(jié)果,該研究表明未接受過(guò)其他治療的病人接受色瑞替尼治療后的中位 PFS 為 16.6 個(gè)月,而接受化療的病人的中位 PFS 僅為 8.1 個(gè)月。色瑞替尼組的藥物緩解率為 73%,高于化療組的 27%。《NCCN 非小細(xì)胞肺癌臨床實(shí)踐指南》(2017.V5) 開始推薦色瑞替尼作為 ALK 陽(yáng)性的晚期 NSCLC 患者的一線治療(證據(jù)等級(jí)1)。
Alectinib 首先于 2014 年在日本上市,用于 ALK 陽(yáng)性的的晚期 NSCLC 患者的治療。在 2015 年年底,Alectinib 被 FDA 批準(zhǔn)用于既往接受克唑替尼后病情進(jìn)展或?qū)诉蛱婺岵荒褪艿?ALK 陽(yáng)性的晚期 NSCLC 患者的治療。在 2017 年 ASCO 會(huì)議上,Alectinib與克唑替尼一線治療的頭對(duì)頭的比較研究中,全面碾壓了克唑替尼。《NCCN 非小細(xì)胞肺癌臨床實(shí)踐指南》(2017.V7)版本,正式確立 Alectinib 為 ALK 陽(yáng)性的 NSCLC 患者一線治療的地位(證據(jù)等級(jí) 1),而且推薦順序排在了克唑替尼、色瑞替尼之前。若有腦轉(zhuǎn)移,一線可考慮直接用色瑞替尼;若沒(méi)有腦轉(zhuǎn)移,可先用克唑替尼,以后再根據(jù)耐藥原因選二三代靶向藥。

X-396是由美國(guó)Xcovery研發(fā)的第二代ALK抑制劑,浙江貝達(dá)藥業(yè)獲得Ensartinib項(xiàng)目在中國(guó)市場(chǎng)的所有權(quán)益。Ensartinib II期臨床部分?jǐn)?shù)據(jù)表明,未用克唑替尼的患者總有效率為88%,PFS最長(zhǎng)已經(jīng)超過(guò)32個(gè)月,進(jìn)展的一名患者為Met擴(kuò)增。克唑替尼耐藥的患者總有效率為77%(10/13),PFS最長(zhǎng)的為29個(gè)月。克唑替尼和色瑞替尼耐藥的患者總有效率為29%。
ALK的第三代靶向藥物是勞拉替尼(Lorlatinib,PF06463922),該藥主要靶向ALK和ROS1,可抑制克唑替尼耐藥的9種突變,幾乎可克服所有耐藥突變,具有較強(qiáng)的血腦屏障透過(guò)能力,入腦效果較強(qiáng),特別適合對(duì)其他ALK耐藥的晚期NSCLC患者。研究發(fā)現(xiàn)ALK的L1198F突變也導(dǎo)致PF-06463922耐藥。
(2) 臨床設(shè)計(jì)及數(shù)據(jù)
表7 ALK抑制劑藥物臨床設(shè)計(jì)及數(shù)據(jù)
藥品名稱:
克唑替尼
獲批時(shí)間及適應(yīng)癥:
克唑替尼分別于 2011 年、2013 年通過(guò) FDA 和 CFDA 批準(zhǔn),用于 ALK 基因融合陽(yáng)性晚期 NSCLC 患者的治療。
臨床試驗(yàn)設(shè)計(jì):
PROFILE1014 研究共納入 343 例 ALK 陽(yáng)性的 NSCLC 患者,其中分別接受克唑替尼治療和一線化療(順鉑 / 卡鉑聯(lián)合培美曲塞)。
實(shí)驗(yàn)數(shù)據(jù):
相比于一線化療組,克唑替尼組同樣顯示了較長(zhǎng)的無(wú)進(jìn)展生存期 PFS(10.9 個(gè)月對(duì)比 7.0 個(gè)月)和較高的藥物緩解率(RR)(74% 對(duì)比 45%)。
獲批時(shí)間及適應(yīng)癥:
2016年適應(yīng)證擴(kuò)展到含有ROS-1基因突變的轉(zhuǎn)移性NSCLC患者,克唑替尼成為第一個(gè)FDA批準(zhǔn)用于ROS-1陽(yáng)性NSCLC患者的治療藥物,也是唯一一個(gè)FDA批準(zhǔn)針對(duì)ROS-1和ALK兩類不同分子靶點(diǎn)的靶向藥物。
臨床試驗(yàn)設(shè)計(jì):
克唑替尼用于治療 ROS-1 陽(yáng)性腫瘤患者的安全性及有效性在一項(xiàng)有 50 名 ROS-1 陽(yáng)性轉(zhuǎn)移性非小細(xì)胞肺癌患者參與的多中心、單組研究中得到評(píng)價(jià)。每天兩次接受克唑替尼治療的患者檢測(cè)這款藥物對(duì)他們肺癌腫瘤的作用。這項(xiàng)研究旨在檢測(cè)總有效率,即腫瘤經(jīng)歷完全或部分縮小的患者百分比。
實(shí)驗(yàn)數(shù)據(jù):
臨床I期,50名受試者每日兩次口服250mg克唑替尼,ORR為72%,包括3例(6%)CR和33例(66%)PR。中位起效時(shí)間為7.9周,中位反應(yīng)持續(xù)時(shí)間為17.6個(gè)月,中位PFS為19.2個(gè)月。中位生存數(shù)據(jù)尚未達(dá)到,12月總生存率為85%。治療的安全性數(shù)據(jù)和ALK陽(yáng)性轉(zhuǎn)移性NSCLC中報(bào)道一致。最常見(jiàn)不良反應(yīng)是視力障礙、惡心、腹瀉、嘔吐、水腫、便秘、轉(zhuǎn)氨酶升高、乏力、食欲下降、上呼吸道感染、頭暈和神經(jīng)病變,94%的不良反應(yīng)為1-2度。
藥品名稱:
色瑞替尼(Ceritinib)
獲批時(shí)間及適應(yīng)癥:
2014年4月抗癌藥Zykadia(ceritinib)獲FDA批準(zhǔn),用于經(jīng)Xalkori(crizotinib)治療后病情惡化或?qū)alkori不耐受的間變性淋巴瘤激酶陽(yáng)性(ALK+)轉(zhuǎn)移性非小細(xì)胞肺癌(NSCLC)患者的治療。
臨床試驗(yàn)設(shè)計(jì):
Zykadi的獲批,是基于一項(xiàng)關(guān)鍵臨床試驗(yàn)的數(shù)據(jù)。該試驗(yàn)在163例經(jīng)Xalkori治療后病情惡化或?qū)alkori不耐受的ALK+NSCLC患者中開展。
實(shí)驗(yàn)數(shù)據(jù):
該研究群體中,腫瘤轉(zhuǎn)移的最常見(jiàn)部位為腦(60%)、肝臟(42%)、骨骼(42%)。研究數(shù)據(jù)表明,Zykadia治療取得了54.6%的總響應(yīng)率(ORR),平均響應(yīng)持續(xù)時(shí)間為7.4個(gè)月。
獲批時(shí)間及適應(yīng)癥:
2017年5月FDA 常規(guī)批準(zhǔn)諾華色瑞替尼用于未經(jīng)治療的間變性淋巴瘤激酶(ALK)陽(yáng)性轉(zhuǎn)移性非小細(xì)胞肺癌(NSCLC)患者,ALK 的狀態(tài)可通過(guò) FDA 批準(zhǔn)的一種檢測(cè)產(chǎn)品進(jìn)行確認(rèn)。
臨床試驗(yàn)設(shè)計(jì):
這次的批準(zhǔn)基于 III期ASCEND-4(NCT01828099)的數(shù)據(jù),這是一項(xiàng)隨機(jī)、多中心、開放式的陽(yáng)性對(duì)照臨床試驗(yàn),受試者為既往未治療的 ALK 陽(yáng)性非小細(xì)胞肺癌患者。所有受試者在中心實(shí)驗(yàn)室以 VENTANA ALK(D5F3)檢測(cè)證實(shí)有 ALK 重排證據(jù)。
ASCEND-4 將 376 名患者按 1:1 的比例配給日服一次的 750 mg 色瑞替尼(n = 189),直到疾病進(jìn)展,或配給鉑類-培美曲塞雙藥化療(n = 187)。化療組患者接受培美曲塞(500 mg/m2)+順鉑(75 mg/m2)或培美曲塞(500 mg/m2)+卡鉑(AUC 5-6)治療,每 21 天為一個(gè)化療周期,每個(gè)周期的第一天進(jìn)行用藥,連續(xù)化療 4 個(gè)周期,隨后以培美曲塞進(jìn)行維持治療。
實(shí)驗(yàn)數(shù)據(jù):
根據(jù) BIRC 的評(píng)價(jià),ASCEND-4 證明受試者的無(wú)進(jìn)展生存期有改善,風(fēng)險(xiǎn)比為 0.55。估計(jì)的色瑞替尼治療組中位數(shù)無(wú)進(jìn)展生存期(PFS)為 16.6 個(gè)月,化療組為 8.1 個(gè)月。色瑞替尼治療組與化療組證實(shí)的總有效率(ORR)分別為 73% 和 27%。色瑞替尼治療組與化療組的估計(jì)中位數(shù)持續(xù)緩解時(shí)間分別為 23.9 個(gè)月和 11.1 個(gè)月。總生存期數(shù)據(jù)尚不成熟。
在基線腦掃描有可檢測(cè)中樞神經(jīng)系統(tǒng)(CNS)損傷的患者中,根據(jù) BIRC 神經(jīng)系放射學(xué)家專家評(píng)估,色瑞替尼治療組證實(shí)總顱內(nèi)緩解率(ORR)為 57%,化療組為 42%。
最常見(jiàn)副作用(ASCEND-4 中至少在 25% 的色瑞替尼治療患者中發(fā)生)是腹瀉、惡心、嘔吐、疲勞、腹痛、食欲下降及咳嗽。38% 的色瑞替尼治療患者中發(fā)生有嚴(yán)重副作用。12% 的患者發(fā)生導(dǎo)致色瑞替尼治療中止的副作用。在 1% 或更多患者中發(fā)生的導(dǎo)致色瑞替尼治療中止的副作用是肌酸酐升高、淀粉酶升高及脂肪酶升高。77% 的患者因副作用而導(dǎo)致劑量中斷,66% 的患者劑量需要減少。色瑞替尼推薦劑量為日服一次 750 mg,至少餐前 1 小時(shí)或餐后 2 小時(shí)服用。
藥品名稱:
Alectinib
獲批時(shí)間及適應(yīng)癥:
2014年在日本上市,2015年12月美國(guó)FDA批準(zhǔn)艾樂(lè)替尼膠囊Alecensa(alectinib)用于治療晚期(轉(zhuǎn)移性)ALK陽(yáng)性非小細(xì)胞肺癌,適用于經(jīng)另一種治療藥物-克唑替尼治療后惡化或不對(duì)其耐受的患者。
臨床試驗(yàn)設(shè)計(jì):
該批準(zhǔn)基于兩項(xiàng)多中心、單臂、開放性臨床研究,總有效率分別為38%、44%,中位緩解時(shí)間分別為7.5個(gè)月、11.5個(gè)月,中樞神經(jīng)系統(tǒng)的總有效率為61%且中位緩解時(shí)間為9.1個(gè)月。推薦劑量為alectinib 600mg bid 與食物同服。最常見(jiàn)副反應(yīng)為乏力、便秘、水腫及肌肉痛,最嚴(yán)重的副反應(yīng)為呼吸困難。
實(shí)驗(yàn)數(shù)據(jù):
臨床研究數(shù)據(jù)在兩個(gè)促成Alecensa批準(zhǔn)的其中一個(gè)研究中,一天兩次用藥,使87名參與者中的38%肺腫瘤縮小,這一效果持續(xù)了平均7個(gè)半月。在第二份研究中(也是由基因泰克資助),138名患者中44%的患者腫瘤縮小了,這一效果持續(xù)了平均大約11個(gè)月。所有參與研究的患者之前都用過(guò)克唑替尼,但是已經(jīng)無(wú)效了。
兩個(gè)研究也都測(cè)試了Alecensa(化學(xué)上稱alectinib 艾樂(lè)替尼)對(duì)已經(jīng)蔓延到大腦的腫瘤的效果,在這類病人中,這種腫瘤轉(zhuǎn)移經(jīng)常發(fā)生。根據(jù)FDA的結(jié)果,兩項(xiàng)研究中61%的患者腦部腫瘤縮小或消失了,效果平均持續(xù)大約九個(gè)月。
獲批時(shí)間及適應(yīng)癥:
2016年10月FDA授予其肺癌新藥Alecensa(alectinib)一線治療成人晚期ALK陽(yáng)性非小細(xì)胞肺癌(NSCLC)突破性藥物資格。
臨床試驗(yàn)設(shè)計(jì):
ALEX 臨床研究是一項(xiàng)隨機(jī)、開放的 Ⅲ 期臨床試驗(yàn),納入了 303 例未經(jīng)治療的 ALK 陽(yáng)性的 NSCLC 患者,其中包括中樞神經(jīng)系統(tǒng)無(wú)癥狀進(jìn)展的患者,隨機(jī)分到克唑替尼組(250 mg/Bid)和 Alectinib 組(600 mg/Bid)進(jìn)行治療。比較了alectinib和克唑替尼作為一線療法的療效和安全性。
實(shí)驗(yàn)數(shù)據(jù):
在經(jīng)過(guò) 17.6 個(gè)月(克唑替尼)和 18.6 個(gè)月(Alectinib)的中位隨訪時(shí)間后,Alectinib 組 12 個(gè)月時(shí)的 PFS 的比例高達(dá) 68.4%,而克唑替尼組的 PFS 的比例只有 48.7%。并且在 24 個(gè)月的時(shí)候,Alectinib 組的 PFS 的比例仍保持在 60% 左右,而克唑替尼組就僅有 20% 左右。2017年ASCO會(huì)議上公布Alectinib中位PFS為25.7個(gè)月,克唑替尼為10.4個(gè)月。12 個(gè)月時(shí),Alectinib 組的中樞神經(jīng)系統(tǒng)進(jìn)展累積發(fā)生率僅為 9.4%,而克唑替尼組則為 41.4%。Alectinib 組的藥物緩解率為 82.9%,也高于克唑替尼組的 75.5%。安全性方面,3~5 級(jí)不良反應(yīng)在 Alectinib 組為 41%,低于克唑替尼組的 50%。
藥品名稱:
Brigatinib
獲批時(shí)間及適應(yīng)癥:
2017年4月brigatinib獲FDA批準(zhǔn)上市。適應(yīng)癥是克唑替尼耐藥的ALK陽(yáng)性的非小細(xì)胞肺癌患者,劑量每天180mg。
FDA是基于一個(gè)數(shù)據(jù)非常出色的二期臨床試驗(yàn)批準(zhǔn)Brigatinib上市。
臨床試驗(yàn)設(shè)計(jì):
臨床試驗(yàn)代號(hào)ALTA臨床設(shè)計(jì):招募222位ALK陽(yáng)性而且使用克唑替尼之后耐藥的晚期非小細(xì)胞肺癌患者,隨機(jī)分成兩組,A組患者每天口服90mg;B組患者前七天每天口服90mg,接下來(lái)每天口服180mg,,中位隨訪時(shí)間8.3個(gè)月。
Ariad已啟動(dòng)代號(hào)為ALTA 1L的III期研究,頭對(duì)頭比較Brigatinib和克唑替尼用于既往未接受過(guò)ALK抑制劑治療的局部晚期或轉(zhuǎn)移性ALK+NSCLC的安全性和療效。
實(shí)驗(yàn)數(shù)據(jù):
A組的客觀緩解率是45%,1名患者腫瘤消失;B組的客觀緩解率是55%,5名患者腫瘤完全消失。AB兩組的疾病控制率都超過(guò)了80%。尤其值得一提的是,對(duì)于腦轉(zhuǎn)移的患者來(lái)說(shuō),A組42%的患者顱內(nèi)腫瘤有明顯縮小,而B組有67%的患者顱內(nèi)腫瘤縮小。
最常見(jiàn)的治療相關(guān)突發(fā)不良事件(TEAEs≥ 25%)包括惡心(40%)、腹瀉(38%)、咳嗽(34%)、血肌酸激酶升高(30%)、頭痛(27%)、疲勞(27%)。3級(jí)以上且發(fā)生率≥ 5%的TEAEs包括血肌酸激酶升高(9%)、高血壓(6%)、肺炎(5%)。
藥品名稱:
X-396
獲批時(shí)間及適應(yīng)癥:
X-396是由Xcovery公司新藥設(shè)計(jì)大師梁從新博士研發(fā)的第2代ALK抑制劑,被美國(guó)列為“抗癌登月計(jì)劃”。
臨床試驗(yàn)設(shè)計(jì):
X-396正在全球70多家醫(yī)院開展III期臨床實(shí)驗(yàn),貝達(dá)藥業(yè)在中大腫瘤防治中心等同步展開臨床試驗(yàn)。X-396屬于第二代的ALK抑制劑,在I、II期臨床中對(duì)ALK陽(yáng)性非小細(xì)胞肺癌有良好的療效和安全性,隨著大規(guī)模III期臨床研究的開展,X-396將成為更具市場(chǎng)潛力的第二代靶向藥。
實(shí)驗(yàn)數(shù)據(jù):
X-396的II期臨床95例患者表明:1、X-396治療克唑替尼(輝瑞)耐藥患者有很好的療效。2、 X-396可有效治療腦轉(zhuǎn),ALK陽(yáng)性患者腦轉(zhuǎn)移的比例很高,克唑替尼(輝瑞)或色瑞替尼(諾華)耐藥且治療失敗的腦轉(zhuǎn)移患者,采用x-396治療腦膜轉(zhuǎn)患者仍有約60%的客觀緩解率。3、x-396也治療其他二代ALK抑制劑(如色瑞替尼(諾華)和阿法替尼)治療后進(jìn)展的患者。4、X-396的耐受性很好,毒副作用輕微,可隨著食物的消化過(guò)程消失。X-396的皮疹和其它靶向藥不同,只要暫停幾天或減量即可。5、X-396對(duì)cmet陽(yáng)性患者也有一定療效。6、目前X-396正和克唑替尼(輝瑞)對(duì)照一線治療ALK陽(yáng)性患者的III 期試驗(yàn),證明 X-396是很有效的藥物,其優(yōu)勢(shì)是相對(duì)于其它靶向藥x-396副作用很低,患者耐受性更好,是目前比較理想的二代靶向藥。
藥品名稱:
勞拉替尼
獲批時(shí)間及適應(yīng)癥:
Lorlatinib 是一個(gè)第三代 ALK/ ROS1 抑制劑,低于納摩爾的劑量就能有效抑制 EML4-ALK 基因重排,其獨(dú)特的大環(huán)結(jié)構(gòu)也使其有更好的血腦屏障穿透能力,目前也是唯一一個(gè)能克服 ALK-G1202R 耐藥位點(diǎn)的 ALK 抑制劑。
臨床試驗(yàn)設(shè)計(jì):
Lorlatinib 于 2017 年 4 月獲 FDA 突破性療法認(rèn)法,用于 ALK 陽(yáng)性的 NSCLC 患者的二線治療。目前也有和克唑替尼比較用于 ALK 陽(yáng)性一線治療轉(zhuǎn)移 NSCLC 患者的臨床試驗(yàn)(NCT03052608)。
II期研究納入了轉(zhuǎn)移性ALK 晚期非小細(xì)胞癌NSCLC患者,至少使用過(guò)一種TKI抑制劑。
實(shí)驗(yàn)數(shù)據(jù):
根據(jù)輝瑞 2016 年 6 月 5 日在 ASCO2016 上公布的I/II期臨床研究數(shù)據(jù)顯示,在 41 例患者接受 lorlatinib 治療的 ALK+ 患者中總應(yīng)答率為 46%,3 例患者實(shí)現(xiàn)完全應(yīng)答,16 例患者實(shí)現(xiàn)部分應(yīng)答(95% CI:31-63),中位 PFS 為 11.4 個(gè)月(95% CI:3.4-16.6)。
最常見(jiàn)的治療相關(guān)不良事件為高膽固醇血癥(69%)和外周性水腫(37%)。最常見(jiàn)的治療相關(guān)的3級(jí)以上不良事件為高膽固醇血癥(11%)。未見(jiàn)患者因?yàn)橹委熛嚓P(guān)不良事件而終止治療。
(3) 耐藥突變
盡管大多數(shù)患者最初受益于克唑替尼,但腫瘤通常在治療后 1 年內(nèi)再次進(jìn)展。目前較為明確的耐藥機(jī)制主要分為2大類:一是 ALK 本身的變化,ALK 基因擴(kuò)增或者 ALK 激酶結(jié)構(gòu)域的繼發(fā)耐藥位點(diǎn);二是旁路途徑的激活,包括其他受體酪氨酸激酶的通路或細(xì)胞下游的信號(hào)通路。
此外血腦屏障的存在是不是克唑替尼的原發(fā)性耐藥機(jī)制一直備受關(guān)注,約有 50% 的患者在接受克唑替尼治療期間會(huì)發(fā)生中樞神經(jīng)系統(tǒng)進(jìn)展。二代或者三代 ALK 抑制一直在這些方面進(jìn)行升級(jí)和改善。
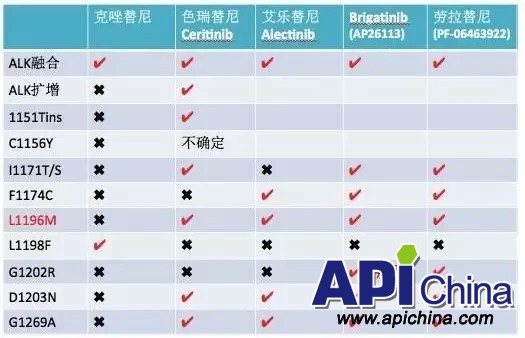
雖然 Brigatinib、Ensartinib(x-396)和 Lorlatinib在臨床試驗(yàn)里顯示了對(duì) G1202R的有效性,但 G1202R突變?cè)诔?Lorlatinib外的 ALK抑制劑耐藥患者中均有存在(表8)。

表8 ALK融合基因陽(yáng)性和二次突變情況

表9 ALK常見(jiàn)變異的靶向藥敏感性
(4) 藥物數(shù)據(jù)對(duì)比
表10 不同 ALK 抑制劑一線治療療效對(duì)比
表11 ALK-TKIs藥物基本信息
藥品名稱:
克唑替尼Crizotinib
研發(fā)公司:輝瑞
分子大小:450
骨架核心:?jiǎn)伟被拎?/p>
服用劑量:250mg,2次/天
FDA批準(zhǔn):一線
藥品名稱:
色瑞替尼ceritinib
研發(fā)公司:諾華
分子大小:558
骨架核心:二氨基吡啶
服用劑量:750mg,1次/天
FDA批準(zhǔn):一線
藥品名稱:
艾樂(lè)替尼aletinib
研發(fā)公司:羅氏
分子大小:483
骨架核心:四環(huán)吲哚
服用劑量:300mg,2次/天
FDA批準(zhǔn):二線
表12 ALK-TKIs一線用藥數(shù)據(jù)
藥品名稱:
克唑替尼
ORR(有效率):75.5%
PFS(耐藥):10.4月
腦轉(zhuǎn)移ORR:26%
重度AE(毒副反應(yīng)):50%
藥品名稱:
色瑞替尼ceritinib
ORR(有效率):72.5%
PFS(耐藥):16.6月
腦轉(zhuǎn)移ORR:46.3%
重度AE(毒副反應(yīng)):78%
藥品名稱:
艾樂(lè)替尼
ORR(有效率):82.9%
PFS(耐藥):25.7月
腦轉(zhuǎn)移ORR:69%
重度AE(毒副反應(yīng)):20%
藥品名稱:
X-396(eXalt2)
ORR(有效率):87%(入組15人)
PFS(耐藥):PFS尚不成熟
腦轉(zhuǎn)移ORR:69%
重度AE(毒副反應(yīng)):20%
表13 ALK-TKIs二、三線用藥數(shù)據(jù)
藥品名稱:
色瑞替尼ceritinib
試驗(yàn)設(shè)計(jì):克唑替尼耐藥后
有效率:56%
PFS:6.9月
腦轉(zhuǎn)移ORR:36%
藥品名稱:
艾樂(lè)替尼Aletinib
試驗(yàn)設(shè)計(jì):克唑替尼耐藥后
有效率:44%
PFS:11.2月
腦轉(zhuǎn)移ORR:61%
藥品名稱:
布加替尼brigatinib
試驗(yàn)設(shè)計(jì):克唑替尼耐藥后
有效率:55%
PFS:15.6月
腦轉(zhuǎn)移ORR:67%
藥品名稱:
X-396(eXalt2)
試驗(yàn)設(shè)計(jì):克唑替尼耐藥后
有效率:71%
PFS:PFS尚不成熟
腦轉(zhuǎn)移ORR:未知
藥品名稱:
勞拉替尼
試驗(yàn)設(shè)計(jì):>=1種TKI耐藥后
有效率:46%
PFS:11.4月
腦轉(zhuǎn)移ORR:未知
總體來(lái)看,相較于克唑替尼,二三代ALK抑制劑可抑制大多數(shù)克唑替尼耐藥的ALK突變;穿透血腦屏障的能力比克唑替尼強(qiáng),顱內(nèi)病灶控制好;繼發(fā)耐藥原因與克唑替尼相似,主要為ALK二次點(diǎn)突變、旁路激活和其他。二代藥物色瑞替尼已經(jīng)獲批作為一線用藥,艾樂(lè)替尼、Brigatinib均有可能成為一線用藥。在研二代藥X-396發(fā)表數(shù)據(jù)不多,初步臨床數(shù)據(jù)顯示,作為一線用藥有效率87%,CNS 響應(yīng)率為 69%,數(shù)據(jù)十分突出,但是臨床入組人數(shù)較少,療效的優(yōu)勢(shì)需要進(jìn)一步通過(guò)臨床試驗(yàn)確認(rèn)。
四、 小結(jié)
NCSLC患者使用各種分子靶向藥后,會(huì)產(chǎn)生耐藥,面對(duì)新出現(xiàn)的耐藥,各種新的靶向藥也一代代開發(fā)出來(lái),NCSLC用藥市場(chǎng)也不斷擴(kuò)大。國(guó)內(nèi)針對(duì)EGFR T790M耐藥突變開發(fā)第三代TKI藥物的企業(yè)甚多,競(jìng)爭(zhēng)十分激烈。在當(dāng)前AZD9291已經(jīng)中國(guó)獲批上市的情況下,國(guó)內(nèi)企業(yè)只有臨床效果優(yōu)于AZD9291(療效更好,副作用更低)或者能夠穿過(guò)血腦屏障的藥物才具備較大的投資價(jià)值。目前,從了解到的信息可知,能夠穿過(guò)血腦屏障的在研藥物包括上海艾利斯的AST2818、韜略生物和鴻運(yùn)華寧共同研發(fā)的GMA204,這些藥物值得關(guān)注。
對(duì)于ALK-TKI來(lái)說(shuō),NSCLC的一線用藥方面,目前艾樂(lè)替尼療效最佳。《NCCN 非小細(xì)胞肺癌臨床實(shí)踐指南》(2017.V7)已經(jīng)正式確立 Alectinib 為 ALK 陽(yáng)性的 NSCLC 患者一線治療的地位。二線用藥方面,2017年4月剛上市的Brigatinib是目前市場(chǎng)上最好的二線用藥。貝達(dá)藥業(yè)和Xcovery研發(fā)的Ensartinib (X-396)初步數(shù)據(jù)顯示,該藥作為一線或二線用藥,有效性數(shù)據(jù)十分搶眼,目前正在臨床III期研究,未來(lái)可能在二線用藥上超越Brigatinib。三線用藥方面,目前僅有輝瑞的第三代ALK抑制劑勞拉替尼(Lorlatinib),該藥可抑制克唑替尼耐藥的9種突變,具有較強(qiáng)的血腦屏障透過(guò)能力,入腦效果較強(qiáng),特別適合對(duì)其他ALK耐藥的晚期NSCLC患者,未來(lái)具有較好的市場(chǎng)前景。Brigatinib、Lorlatinib和Ensartinib一線PK克唑替尼的三期臨床試驗(yàn)正在進(jìn)行,在接下來(lái)的2-3年里,ALK抑制劑領(lǐng)域?qū)?huì)有效果更好的一線藥物出現(xiàn)。
隨著人們對(duì)分子遺傳學(xué)認(rèn)識(shí)的不斷增強(qiáng),NSCLC 被細(xì)分為各種不同的分子亞型,并由此誕生了各類分子靶向治療藥物。靶向藥的應(yīng)用,明顯改善了 NSCLC 患者的預(yù)后。非小細(xì)胞肺癌不再被視為一個(gè)疾病,它是一類由不同分子亞型構(gòu)成的異質(zhì)性疾病。對(duì)非小細(xì)胞肺癌患者進(jìn)行組織活檢來(lái)測(cè)定 EGFR 和 ALK 狀態(tài)已經(jīng)是一個(gè)重要的診療步驟。
雖然本綜述僅僅論述了分子靶向治療和相關(guān)的癌驅(qū)動(dòng)基因,市場(chǎng)上還有很多其他的靶向治療方案。比如貝伐單抗(一種抗血管生成劑)聯(lián)合紫杉醇 + 鉑類治療可以改善患者總生存期。另一個(gè)重要的治療手段是分子調(diào)節(jié)免疫應(yīng)答。隨著腫瘤免疫生物學(xué)研究的不斷推進(jìn),新的免疫療法正在飛速發(fā)展。比如免疫檢查點(diǎn)藥物PD-1抑制劑Keytruda被FDA批準(zhǔn)同時(shí)作為單藥和聯(lián)合療法用于轉(zhuǎn)移性非小細(xì)胞肺癌的一線治療。另外,F(xiàn)DA已批準(zhǔn)Opdivo用于二線治療NSCLC,Tecentriq用于接受含鉑化療治療期間或治療后病情進(jìn)展、以及接受靶向療法(若腫瘤中存在EGFR或ALK基因異常)治療失敗的轉(zhuǎn)移性非小細(xì)胞肺癌。